肉腫の融合遺伝子とその標的分子の機能を明らかにする
京都大学 工学部・大学院工学研究所
マイクロエンジニアリング専攻の 横川隆司 教授は、東京医科大学の 中村卓郎 特任教授、公益財団法人がん研究会の 田中美和 主任研究員、 丸山玲緒 プロジェクトリーダー、がん研有明病院の 阿江啓介 整形外科部長、松本誠一 サルコーマセンター長らとの共同研究で、胞巣状軟部肉腫(alveolar soft part sarcoma, ASPS)の原因融合遺伝子ASPSCR1::TFE3(AT3)の機能とその標的遺伝子を明らかにし、ASPSの血管形成を誘導する仕組みを解明しました。
ASPSは希少がんである軟部肉腫の一つで、AYA世代(思春期・若年成人)に好発します。腫瘍の増殖は緩やかですが、血管形成が盛んなことから全身に転移する傾向が強く、予後不良な疾患です。ASPSの原因融合遺伝子AT3が血管形成をはじめとする腫瘍の形質をコントロールしていることが示唆されていました。本研究グループは2017年にASPSのマウスモデルを確立して研究を進めていましたが、今回AT3蛋白質が血管形成を促進する遺伝子のスーパーエンハンサーに結合することを発見し、エピゲノム編集技術を用いて標的遺伝子を同定しました。標的遺伝子には血管形成因子自体と、それらを運ぶ細胞内輸送促進因子が含まれ、ASPSにおける独特な血管構造の原因となっていることがわかりました。今後、輸送促進因子機能を抑える全く新しい治療方法の開発にもつながる成果と期待されます。
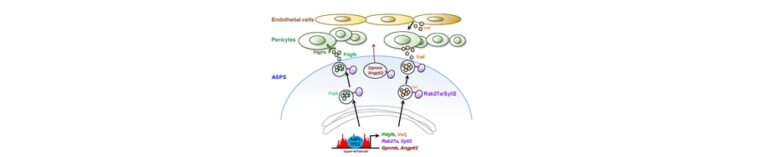
AT3による標的遺伝子を介した血管新生機構
・研究詳細
がんにおける新たな血管新生機構を発見 ー肉腫の融合遺伝子とその標的分子の機能を明らかにする ー
・研究者情報
横川 隆司 京都大学教育研究活動データベース
・書籍情報
タイトル:ASPSCR1:TFE3 orchestrates the angiogenic program of alveolar soft part sarcoma
著者:田中美和、Surachada Chuaychob、本目みずき、山崎ゆかり、Ruyin Lyu、山下享子、阿江啓介、松本誠一、粂川昂平、丸山玲緒、Wei Qu、宮城洋平、横川隆司、中村卓郎
掲載誌:Nature Communications